Innholdsfortegnelse for denne artikkelen:
1. Utvikling av aminosyrer
2. Strukturelle egenskaper
3. Kjemisk sammensetning
4. Klassifisering
5. Syntese
6. Fysisk -kjemiske egenskaper
7. Toksisitet
8. Antimikrobiell aktivitet
9. Revologiske egenskaper
10. Søknader i kosmetikkindustrien
11. Søknader i hverdagskosmetikk
Aminosyre Surfactants (AAS)er en klasse av overflateaktive midler dannet ved å kombinere hydrofobe grupper med en eller flere aminosyrer. I dette tilfellet kan aminosyrene være syntetiske eller avledet fra proteinhydrolysater eller lignende fornybare kilder. Denne artikkelen dekker detaljene i de fleste av de tilgjengelige syntetiske rutene for AAS og effekten av forskjellige ruter på de fysisk -kjemiske egenskapene til sluttproduktene, inkludert løselighet, spredningsstabilitet, toksisitet og biologisk nedbrytbarhet. Som en klasse av overflateaktive midler i økende etterspørsel, gir allsidigheten til AAS på grunn av deres variable struktur et stort antall kommersielle muligheter.
Gitt at overflateaktive midler er mye brukt i vaskemidler, emulgatorer, korrosjonshemmere, utvinning av tertiær olje og legemidler, har forskere aldri sluttet å ta hensyn til overflateaktive midler.
Surfaktanter er de mest representative kjemiske produktene som konsumeres i store mengder på daglig basis rundt om i verden og har hatt en negativ innvirkning på vannmiljøet.Studier har vist at den utbredte bruken av tradisjonelle overflateaktive midler kan ha en negativ innvirkning på miljøet.
I dag er ikke-giftighet, biologisk nedbrytbarhet og biokompatibilitet nesten like viktig for forbrukerne som nytten og ytelsen til overflateaktive midler.
Biosurfaktanter er miljøvennlige bærekraftige overflateaktive midler som naturlig syntetiseres av mikroorganismer som bakterier, sopp og gjær, eller utskilt ekstracellulært.Derfor kan biosurfaktanter også fremstilles ved molekylær design for å etterligne naturlige amfifile strukturer, så som fosfolipider, alkylglykosider og acylaminosyrer.
Aminosyre Surfactants (AAS)er en av de typiske overflateaktive midlene, vanligvis produsert fra dyre- eller landbruksavledede råvarer. I løpet av de siste to tiårene har AAS tiltrukket seg stor interesse fra forskere som nye overflateaktive midler, ikke bare fordi de kan syntetiseres fra fornybare ressurser, men også fordi AAS lett er nedbrytbare og har ufarlige biprodukter, noe som gjør dem tryggere for miljøet.
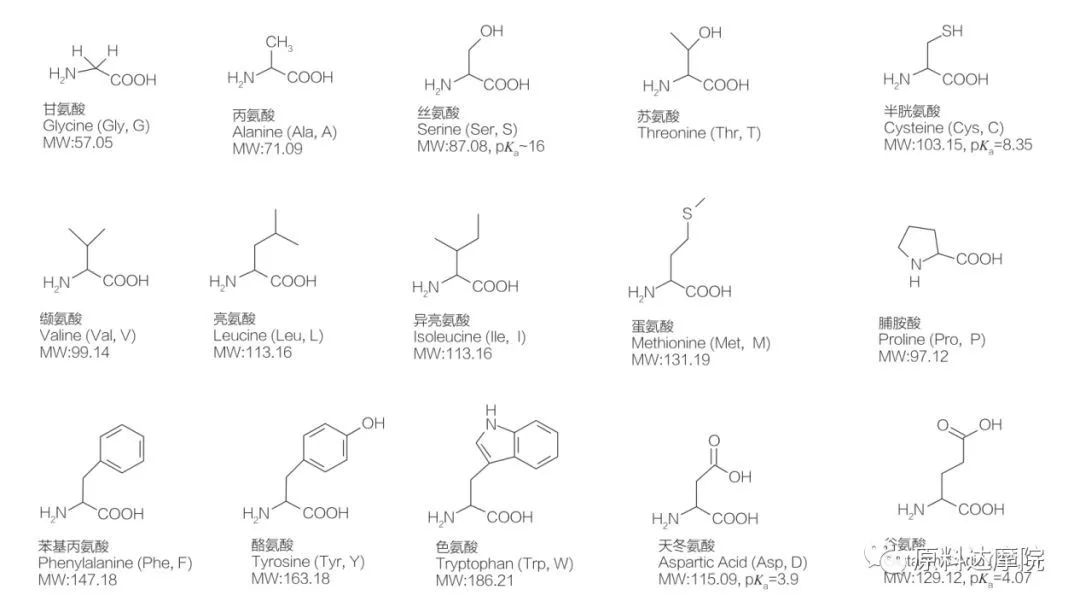
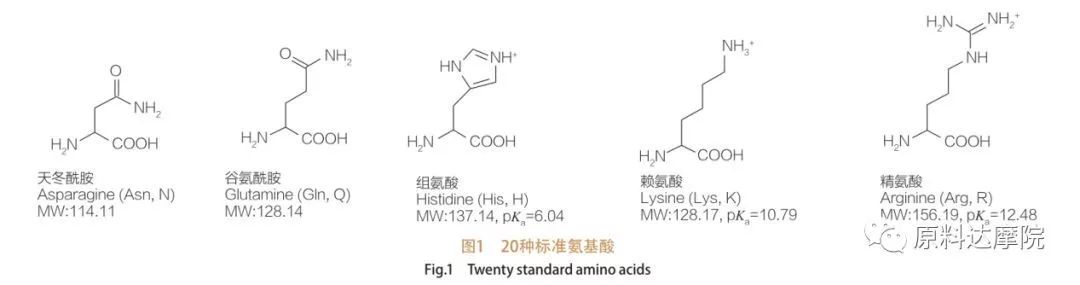
AA-er kan defineres som en klasse av overflateaktive midler bestående av aminosyrer som inneholder aminosyregrupper (HO 2 C-CHR-NH 2) eller aminosyrerester (HO 2 C-CHR-NH-). De to funksjonelle regionene av aminosyrer muliggjør avledning av et bredt utvalg av overflateaktive midler. Totalt 20 standard proteinogene aminosyrer er kjent for å eksistere i naturen og er ansvarlige for alle fysiologiske reaksjoner i vekst- og livsaktiviteter. De skiller seg fra hverandre bare i henhold til resten R (figur 1, PK A er den negative logaritmen til syredissosiasjonskonstanten til løsningen). Noen er ikke-polare og hydrofobe, andre er polare og hydrofile, noen er basiske og noen er sure.
Fordi aminosyrer er fornybare forbindelser, har overflateaktive midler syntetisert fra aminosyrer også et stort potensial til å bli bærekraftig og miljøvennlig. Den enkle og naturlige strukturen, lav toksisitet og rask biologisk nedbrytbarhet gjør dem ofte overlegne overfor konvensjonelle overflateaktive midler. Ved hjelp av fornybare råvarer (f.eks. Aminosyrer og vegetabilske oljer) kan AAS produseres ved forskjellige bioteknologiske ruter og kjemiske ruter.
På begynnelsen av 1900 -tallet ble aminosyrer først oppdaget å bli brukt som underlag for syntese av overflateaktive midler.AAS ble hovedsakelig brukt som konserveringsmidler i farmasøytiske og kosmetiske formuleringer.I tillegg ble AAS funnet å være biologisk aktive mot en rekke sykdomsfremkallende bakterier, svulster og virus. I 1988 genererte tilgjengeligheten av lavpris AAS forskningsinteresse for overflateaktivitet. I dag, med utviklingen av bioteknologi, kan noen aminosyrer også syntetiseres kommersielt i stor skala av gjær, som indirekte beviser at AAS -produksjon er mer miljøvennlig.
01 Utvikling av aminosyrer
Allerede på begynnelsen av 1800 -tallet, da naturlig forekommende aminosyrer først ble oppdaget, ble strukturene deres spådd å være ekstremt verdifulle - brukbare som råvarer for fremstilling av amfifiler. Den første studien på syntesen av AAS ble rapportert av Bondi i 1909.
I den studien ble N-acylglycin og N-acylalanin introdusert som hydrofile grupper for overflateaktive midler. Etterfølgende arbeid involverte syntese av lipoaminosyrer (AAS) ved bruk av glycin og alanin, og Hentrich et al. publiserte en serie funn,Inkludert den første patentsøknaden, om bruk av acylsarkosinat og acylaspartatsalter som overflateaktive midler i husholdningsrengjøringsprodukter (f.eks. Sjampo, vaskemidler og tannkrem).Deretter undersøkte mange forskere syntesen og fysisk -kjemiske egenskapene til acylaminosyrer. Til dags dato er det publisert et stort antall litteratur om syntese, egenskaper, industrielle applikasjoner og biologisk nedbrytbarhet av AAS.
02 Strukturelle egenskaper
De ikke-polare hydrofobe fettsyrekjeder av AA-er kan variere i struktur, kjedelengde og antall.Det strukturelle mangfoldet og den høye overflateaktiviteten til AA -er forklarer deres brede komposisjonsmangfold og fysisk -kjemiske og biologiske egenskaper. Hodegruppene til AAS er sammensatt av aminosyrer eller peptider. Forskjellene i hodegruppene bestemmer adsorpsjon, aggregering og biologisk aktivitet av disse overflateaktive midlene. De funksjonelle gruppene i hodegruppen bestemmer deretter typen AA -type, inkludert kationiske, anioniske, ikke -ioniske og amfoteriske. Kombinasjonen av hydrofile aminosyrer og hydrofobe langkjedede deler danner en amfifil struktur som gjør molekylet svært overflate aktivt. I tillegg hjelper tilstedeværelsen av asymmetriske karbonatomer i molekylet til å danne chirale molekyler.
03 Kjemisk sammensetning
Alle peptider og polypeptider er polymerisasjonsproduktene til disse nesten 20 a-proteinogene a-aminosyrene. Alle 20 a-aminosyrer inneholder en funksjonell gruppe for karboksylsyre (-COOH) og en amino-funksjonell gruppe (-NH 2), begge festet til det samme tetrahedrale a-karbonatom. Aminosyrer skiller seg fra hverandre av de forskjellige R-gruppene som er festet til a-karbon (bortsett fra lycine, der R-gruppen er hydrogen.) R-gruppene kan avvike i struktur, størrelse og ladning (surhet, alkalinitet). Disse forskjellene bestemmer også løseligheten av aminosyrer i vann.
Aminosyrer er chirale (bortsett fra glycin) og er optisk aktive av natur fordi de har fire forskjellige substituenter knyttet til alfakarbonet. Aminosyrer har to mulige konformasjoner; De er ikke-overlappende speilbilder av hverandre, til tross for at antallet L-stereoisomerer er betydelig høyere. R-gruppen som er til stede i noen aminosyrer (fenylalanin, tyrosin og tryptofan) er aryl, noe som fører til en maksimal UV-absorpsjon ved 280 nm. Den sure a-COOH og de grunnleggende a-NH2 i aminosyrene er i stand til ionisering, og begge stereoisomerer, avhengig av hva de er, konstruerer ioniserings likevekten vist nedenfor.
R-COOH ↔r-Coo-+ H.+
R-nh3+↔r-nh2+ H.+
Som vist i ioniserings likevekten ovenfor, inneholder aminosyrer minst to svakt sure grupper; Imidlertid er karboksylgruppen mye surere sammenlignet med den protonerte aminogruppen. PH 7.4, karboksylgruppen blir avprotonert mens aminogruppen er protonert. Aminosyrer med ikke-ioniserbare R-grupper er elektrisk nøytrale ved denne pH og danner zwitterion.
04 Klassifisering
AAS kan klassifiseres i henhold til fire kriterier, som er beskrevet nedenfor etter tur.
4.1 I henhold til opprinnelsen
| I følge opprinnelsen kan AAS deles inn i to kategorier som følger. ① Naturlig kategori Noen naturlig forekommende forbindelser som inneholder aminosyrer har også evnen til å redusere overflate/grensesnittspenning, og noen overskrider til og med effekten av glykolipider. Disse AA -ene er også kjent som lipopeptider. Lipopeptider er forbindelser med lav molekylvekt, vanligvis produsert av Bacillus -arter.
Slike AA -er er videre delt inn i 3 underklasser:Surfactin, Iturin og Fengycin.
|
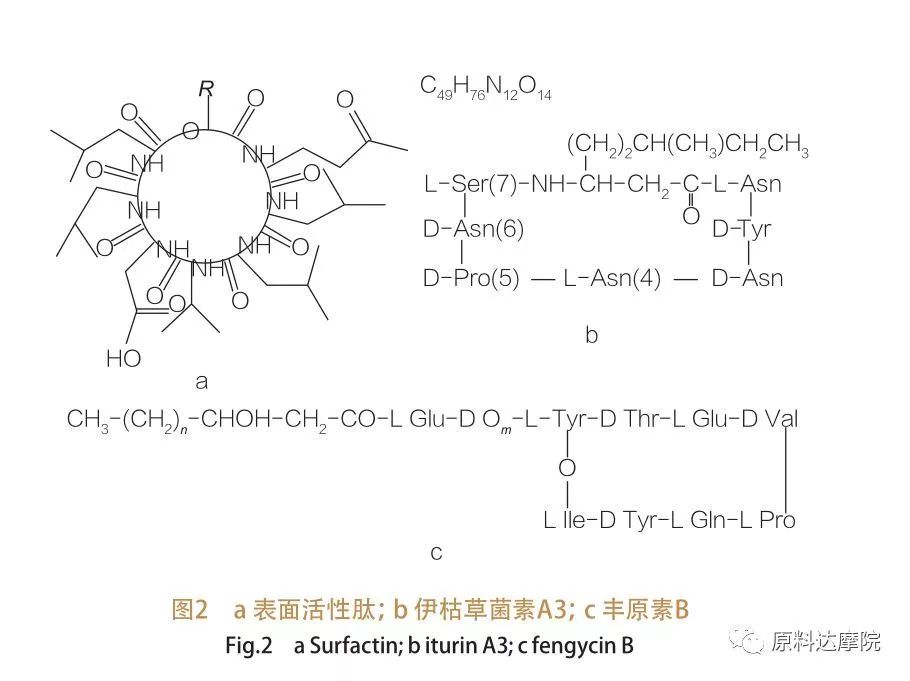
| Familien med overflateaktive peptider omfatter heptapeptidvarianter av en rekke stoffer,som vist i figur 2A, der en C12-C16 umettet ß-hydroksy fettsyrekjede er knyttet til peptidet. Det overflateaktive peptidet er en makrosyklisk lakton der ringen lukkes ved katalyse mellom C-terminalen til ß-hydroksy-fettsyren og peptidet. I underklassen til iturin er det seks hovedvarianter, nemlig iturin A og C, Mycosubtilin og Bacillomycin D, F og L.I alle tilfeller er heptapeptidene knyttet til C14-C17-kjedene til ß-amino-fettsyrer (kjedene kan være forskjellige). Når det gjelder Ekurimycins, kan aminogruppen ved ß-posisjonen danne en amidbinding med C-terminalen og dermed danne en makrocyklisk laktamstruktur.
Underklassen Fengycin inneholder fengycin A og B, som også kalles plipastatin når Tyr9 er D-konfigurert.Dekapeptidet er koblet til en C14 -C18 mettet eller umettet ß -hydroksy fettsyrekjede. Strukturelt er plipastatin også en makrosyklisk lakton, som inneholder en Tyr-sidekjede i posisjon 3 av peptidsekvensen og danner en esterbinding med den C-terminale rest, og danner dermed en intern ringstruktur (som tilfellet er for mange Pseudomonas lipopeptider).
② Syntetisk kategori AAS kan også syntetiseres ved å bruke hvilken som helst av de sure, basiske og nøytrale aminosyrene. Vanlige aminosyrer som brukes til syntese av AA -er er glutaminsyre, serin, prolin, aspartinsyre, glycin, arginin, alanin, leucin og proteinhydrolysater. Denne underklassen av overflateaktive midler kan fremstilles ved kjemiske, enzymatiske og kjemoenzymatiske metoder; For produksjon av AAS er imidlertid kjemisk syntese mer økonomisk gjennomførbar. Vanlige eksempler inkluderer N-LaUroyl-L-glutaminsyre og N-palmitoyl-L-glutaminsyre.
|
4.2 Basert på alifatiske kjedesubstituenter
Basert på de alifatiske kjedesubstituentene, kan aminosyrebaserte overflateaktive midler deles inn i 2 typer.
I henhold til substituentens posisjon
| ①N-substituert AAS I N-substituerte forbindelser erstattes en aminogruppe av en lipofil gruppe eller en karboksylgruppe, noe som resulterer i tap av basisitet. Det enkleste eksemplet på N-substituerte AA-er er N-acyl aminosyrer, som i hovedsak er anioniske overflateaktive midler. N-substituert AAS har en amidbinding festet mellom de hydrofobe og hydrofile porsjonene. Amidbindingen har evnen til å danne en hydrogenbinding, noe som letter nedbrytningen av dette overflateaktivt middel i et surt miljø, og dermed gjør det biologisk nedbrytbart.
②C-substituert AAS I C-substituerte forbindelser skjer substitusjonen ved karboksylgruppen (via en amid eller esterbinding). Typiske C-substituerte forbindelser (f.eks. Estere eller amider) er i hovedsak kationiske overflateaktive stoffer.
③N- og C-substituerte AAS I denne typen overflateaktivt middel er både amino- og karboksylgruppene den hydrofile delen. Denne typen er egentlig et amfoterisk overflateaktivt middel. |
4.3 I henhold til antall hydrofobe haler
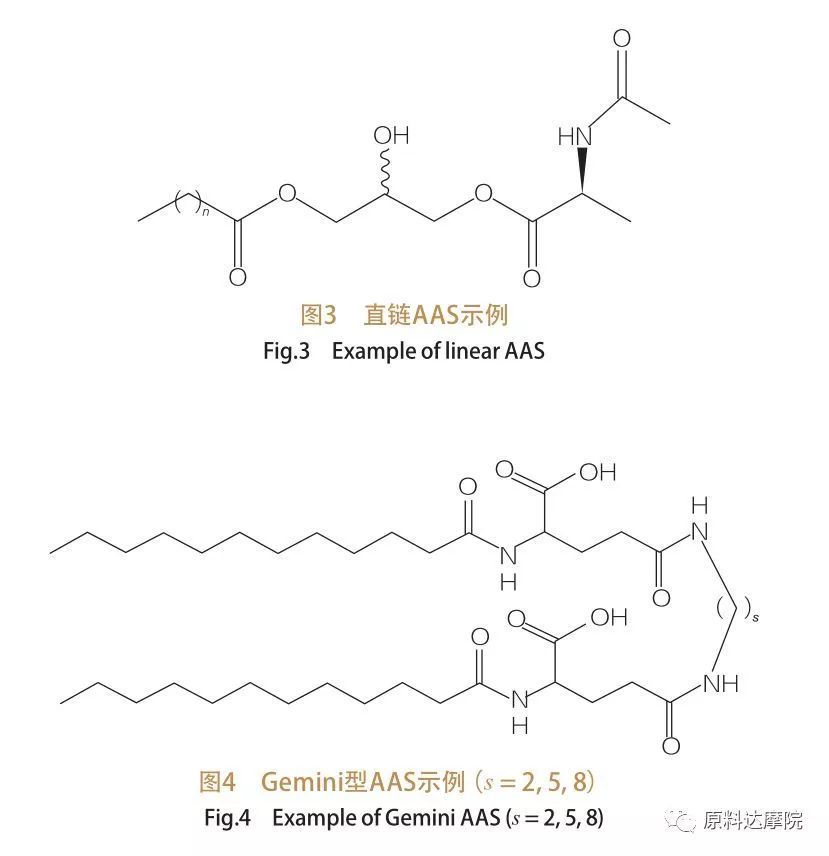
Basert på antall hodegrupper og hydrofobe haler, kan AAS deles inn i fire grupper. Rettkjede AAS, Gemini (Dimer) Type AAS, Glycerolipid Type AAS og Bicephalic Amphiphilic (Bola) Type AAS. Rettkjedede overflateaktive midler er overflateaktive midler som består av aminosyrer med bare en hydrofob hale (figur 3). Gemini Type AAS har to aminosyrer polare hodegrupper og to hydrofobe haler per molekyl (figur 4). I denne typen strukturer er de to rettkjede AA-ene koblet sammen av en avstandsstykker og kalles derfor også dimerer. I Glycerolipid -typen AAS, derimot, er de to hydrofobe halene festet til den samme aminosyrehodegruppen. Disse overflateaktive midlene kan betraktes som analoger av monoglyserider, diglyserider og fosfolipider, mens i Bola-type AA-er, er to aminosyrehodegrupper koblet med en hydrofob hale.
4.4 I henhold til type hodegruppe
①Cationic AAS
Hovedgruppen for denne typen overflateaktivt middel har en positiv ladning. Den tidligste kationiske AAS er etyl cocoyl arginat, som er et pyrrolidonkarboksylat. De unike og mangfoldige egenskapene til dette overflateaktivt middel gjør det nyttig hos desinfeksjonsmidler, antimikrobielle midler, antistatiske midler, hårbalsam, i tillegg til å være skånsomme mot øynene og huden og lett biologisk nedbrytbar. Singare og Mhatre syntetiserte argininbaserte kationiske AA-er og evaluerte deres fysisk-kjemiske egenskaper. I denne studien hevdet de høye avkastninger av produktene oppnådd ved bruk av Schotten-Baumann-reaksjonsbetingelser. Med økende alkylkjedelengde og hydrofobisitet, ble overflateaktiviteten til det overflateaktive middelet funnet å øke og den kritiske micellkonsentrasjonen (CMC) for å avta. En annen er det kvartære acylproteinet, som ofte brukes som balsam i hårpleieprodukter.
②Anionic AAS
I anioniske overflateaktive stoffer har den polare hodegruppen av overflateaktivt middel en negativ ladning. Sarkosin (CH 3 -NH -CH 2 -COOH, N -metylglycin), en aminosyre som ofte finnes i kråkeboller og sjøstjerner, er kjemisk relatert til glycin (NH 2 -CH 2 -COOH,), en basisk aminosyre funnet i pattedyrceller. -COOH,) er kjemisk relatert til glycin, som er en basisk aminosyre som finnes i pattedyrceller. Laurinsyre, tetradecansyre, oljesyre og deres halogenider og estere blir ofte brukt til å syntetisere sarkosinatoverflater. Sarkosinater er iboende milde og brukes derfor ofte i munnskyll, sjampo, spraybarberingsskum, solkremer, hudrensere og andre kosmetiske produkter.
Andre kommersielt tilgjengelige anioniske AA-er inkluderer Amisoft CS-22 og Amilitegck-12, som er handelsnavn for henholdsvis natrium N-cocoyl-L-glutamat og kalium N-cocoyl glykcinat. Amilitt brukes ofte som et skummende middel, vaskemiddel, solubilisator, emulgator og dispergeringsmiddel, og har mange bruksområder innen kosmetikk, som sjampo, badesåper, kroppsvasker, tannkrem, ansiktsrensere, rensende såper, kontaktlinserensere og husholdningsoverflate. Amisoft brukes som en mild hud- og hårrens, hovedsakelig i ansikts- og kroppsrensere, blokkerer syntetiske vaskemidler, kroppspleieprodukter, sjampoer og andre hudpleieprodukter.
③zwitterionic eller amfoterisk AAS
Amfoteriske overflateaktive midler inneholder både sure og grunnleggende steder og kan derfor endre ladningen ved å endre pH -verdien. I alkaliske medier oppfører de seg som anioniske overflateaktive midler, mens de i sure miljøer oppfører seg som kationiske overflateaktive midler og i nøytrale medier som amfoteriske overflateaktive midler. Lauryl lysine (LL) og alkoxy (2-hydroxypropyl) arginin er de eneste kjente amfoteriske overflateaktive midler basert på aminosyrer. LL er et kondensasjonsprodukt av lysin og laurinsyre. På grunn av sin amfoteriske struktur er LL uoppløselig i nesten alle typer løsningsmidler, bortsett fra veldig alkaliske eller sure løsningsmidler. Som et organisk pulver har LL utmerket vedheft til hydrofile overflater og en lav friksjonskoeffisient, noe som gir denne overflateaktivt middel utmerket smøreevne. LL er mye brukt i hudkremer og hårbalsam, og brukes også som smøremiddel.
④Nonionic AAS
Ikke -ioniske overflateaktive midler er preget av polare hodegrupper uten formelle ladninger. Åtte nye etoksylerte ikke-ioniske overflateaktive midler ble fremstilt av Al-Sabagh et al. fra oljeløs α-aminosyrer. I denne prosessen ble L-fenylalanin (LEP) og L-leucin først forestret med heksadekanol, fulgt av amidering med palmitinsyre for å gi to amider og to estere av a-aminosyrer. Amidene og estere gjennomgikk deretter kondensasjonsreaksjoner med etylenoksyd for å fremstille tre fenylalaninderivater med forskjellige antall polyoksyetylenenheter (40, 60 og 100). Disse ikke -ioniske AA -ene ble funnet å ha gode vaskemidler og skummende egenskaper.
05 Syntese
5.1 Grunnleggende syntetisk rute
I AAS kan hydrofobe grupper festes til amin- eller karboksylsyresteder, eller gjennom sidekjedene til aminosyrer. Basert på dette er fire grunnleggende syntetiske ruter tilgjengelige, som vist i figur 5.
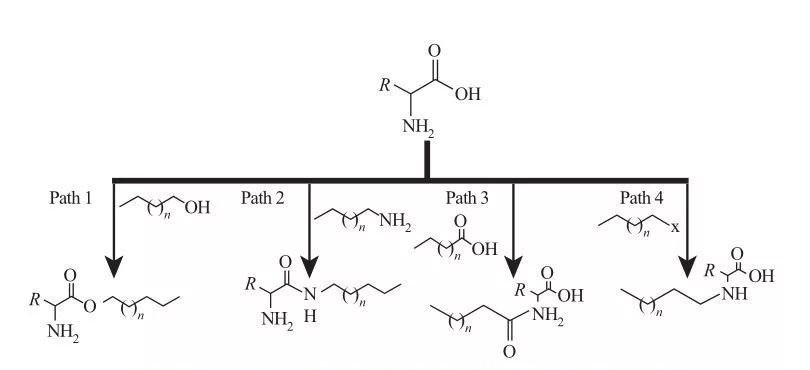
Fig.5 Grunnleggende synteseveier for aminosyrebaserte overflateaktive stoffer
| Bane 1. Amfifile esteraminer produseres ved esterifiseringsreaksjoner, i hvilket tilfelle oppnås overflateaktivt middel -syntese ved å reflektere fettholdige alkoholer og aminosyrer i nærvær av et dehydrerende middel og en sur katalysator. I noen reaksjoner fungerer svovelsyre som både en katalysator og et dehydrerende middel.
Bane 2. Aktiverte aminosyrer reagerer med alkylaminer for å danne amidbindinger, noe som resulterer i syntese av amfifile amidoaminer.
Bane 3. Amidosyrer syntetiseres ved å reagere aminegruppene av aminosyrer med amidosyrer.
Bane 4. Langkjedede alkylaminosyrer ble syntetisert ved reaksjonen fra amingrupper med haloalkaner. |
5.2 Fremskritt i syntese og produksjon
5.2.1 Syntese av enkjede aminosyre/peptid overflateaktive midler
N-acyl eller O-acyl aminosyrer eller peptider kan syntetiseres ved enzymkatalysert acylering av amin- eller hydroksylgrupper med fettsyrer. Den tidligste rapporten om det løsningsmiddelfrie lipasekatalysert syntese av aminosyreamid- eller metylesterderivater brukte Candida Antarktis, med utbytter fra 25% til 90% avhengig av målaminosyren. Metyletylketon har også blitt brukt som et løsningsmiddel i noen reaksjoner. Vonderhagen et al. Også beskrevne lipase- og proteasikatalyserte N-acyleringsreaksjoner av aminosyrer, proteinhydrolysater og/eller deres derivater ved bruk av en blanding av vann og organiske løsningsmidler (f.eks. Dimetylformamid/vann) og metylbutyleton.
I de første dagene var hovedproblemet med enzymkatalysert syntese av AAS de lave utbyttet. I følge Valivety et al. Utbyttet av N-tetradecanoyl aminosyrderivater var bare 2% -10% selv etter å ha brukt forskjellige lipaser og inkubering ved 70 ° C i mange dager. Montet et al. Også har problemer med det lave utbyttet av aminosyrer i syntesen av N-Acyl-lysin ved bruk av fettsyrer og vegetabilske oljer. I følge dem var det maksimale utbyttet av produktet 19% under løsningsmiddelfrie forhold og bruk av organiske løsningsmidler. Det samme problemet ble opplevd av Valivety et al. i syntesen av N-CBZ-L-lysin eller N-CBZ-lysin metylesterderivater.
I denne studien hevdet de at utbyttet av 3-O-tetradecanoyl-L-serin var 80% når man brukte N-beskyttet serin som et underlag og novozyme 435 som en katalysator i et smeltet løsningsmiddelfritt miljø. Nagao og Kito studerte O-acylering av L-serin, L-homoserin, L-Threonin og L-tyrosin (Let) når du brukte lipase, resultatene av reaksjonen (lipase ble oppnådd ved candida sylindracea og rhizopus delemar i vandig buffer og rapportert at utbyttet av Acylation av Acylation av l-sor-sor-sor-sor-sor-sor-sor-sor-sor-sor-sor-ser-ser-ser-ser-ser-serle-sero-syl-serle-sero-syling var en ACYL-sylindratee og en Acyls-syl-serisk-syl-syling som var en low-syl-syl-syl-syl-syl-serol-sylindrasse og riryl. av l-threonin og la oppstod.
Mange forskere har støttet bruken av billige og lett tilgjengelige underlag for syntese av kostnadseffektive AA-er. Soo et al. hevdet at utarbeidelsen av palmeoljebaserte overflateaktive midler fungerer best med immobilisert lipoenzym. De bemerket at utbyttet av produktene ville være bedre til tross for den tidkrevende reaksjonen (6 dager). Gerova et al. undersøkte syntesen og overflateaktiviteten til chiral N-palmitoyl AAS basert på metionin, prolin, leucin, treonin, fenylalanin og fenylglycin i en syklisk/racemisk blanding. Pang og Chu beskrev syntesen av aminosyrebaserte monomerer og dikarboksylsyrebaserte monomerer i løsning en serie funksjonelle og biologisk nedbrytbare aminosyrebaserte polyamidestere ble syntetisert ved co-kondensasjonsreaksjoner i løsning.
Cantaeuzene og Guerreiro rapporterte forestring av karboksylsyregrupper av Boc-Ala-OH og Boc-Asp-OH med langkjedede alifatiske alkoholer og dioler, med diklormetan som løsningsmiddel og agarose 4B (Sepharose 4B) som katalysator. I denne studien ga reaksjonen av BOC-ala-OH med fete alkoholer opp til 16 karbonatomer gode utbytter (51%), mens for BOC-ASP-OH 6 og 12 karbonatomer var bedre, med et tilsvarende utbytte på 63% [64]. 99,9%) i avkastning fra 58%til 76%, som ble syntetisert ved dannelse av amidbindinger med forskjellige langkjedede alkylaminer eller esterbindinger med fettalkoholer av CBZ-Arg-OMe, hvor papain fungerte som en katalysator.
5.2.2 Syntese av Gemini-baserte aminosyre/peptid overflateaktive midler
Aminosyrebaserte Gemini-overflateaktive midler består av to rettkjede AAS-molekyler koblet head-to-head til hverandre av en spacer-gruppe. Det er to mulige ordninger for kjemoenzymatisk syntese av aminosyrebaserte overflateaktive midler av gemini-type (figur 6 og 7). I figur 6 blir 2 aminosyrederivater reagert med forbindelsen som en avstandsgruppe og deretter introduseres 2 hydrofobe grupper. I figur 7 er de to rettkjedede strukturene direkte koblet sammen av en bifunksjonell avstandsgruppe.
Den tidligste utviklingen av enzymkatalysert syntese av Gemini Lipoaminosyrer ble pioner av Valivety et al. Yoshimura et al. undersøkte syntese, adsorpsjon og aggregering av et aminosyrebasert Gemini-overflateaktivt middel basert på cystin og N-alkylbromid. De syntetiserte overflateaktive midlene ble sammenlignet med de tilsvarende monomere overflateaktive stoffer. Faustino et al. beskrev syntesen av anionisk urea-basert monomer AAS basert på L-cystin, D-cystin, DL-cystin, L-cystein, L-metionin og L-sulfoalanin og deres par av Gemini ved hjelp av ledning, likevektsflate og stabilinstasjonsrekkevekt av dem. Det ble vist at CMC -verdien til Gemini var lavere ved å sammenligne monomer og Gemini.
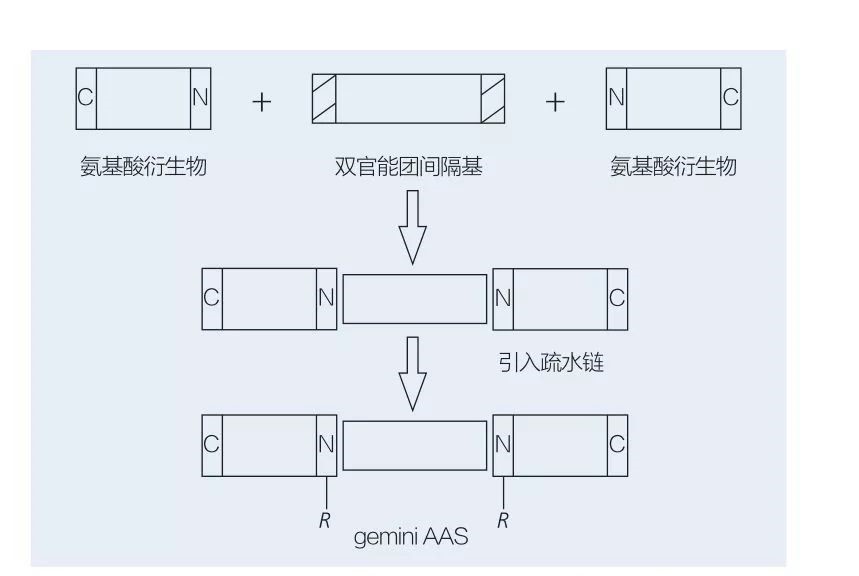
Fig.6 Syntese av Gemini AAS ved bruk av AA -derivater og avstandsstykker, etterfulgt av innsetting av den hydrofobe gruppen
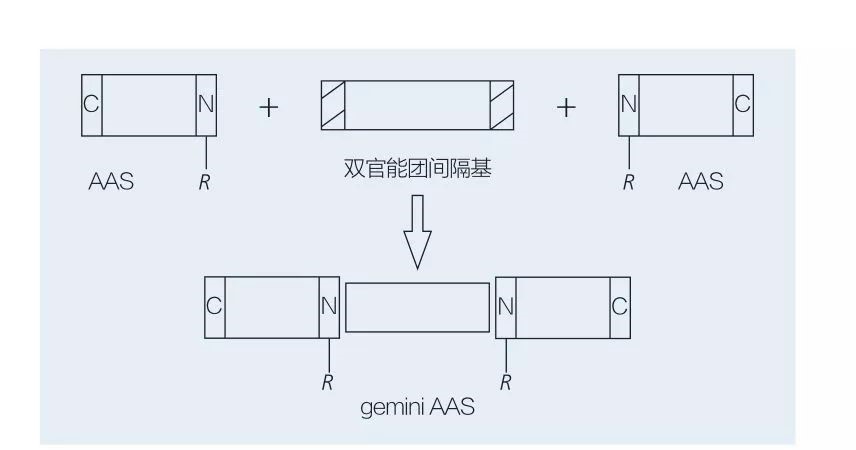
Fig.7 Syntese av Gemini Aass ved bruk av bifunksjonell avstand og AAS
5.2.3 Syntese av glyserolipid aminosyre/peptid overflateaktive midler
Glycerolipid aminosyre/peptid overflateaktive midler er en ny klasse av lipidaminosyrer som er strukturelle analoger av glyserolmono- (eller di-) estere og fosfolipider, på grunn av deres struktur av en eller to fettkjeder med en aminosyre koblet til glyserolryggen av en estbinding. Syntesen av disse overflateaktive midlene starter med fremstilling av glyserolestere av aminosyrer ved forhøyede temperaturer og i nærvær av en sur katalysator (f.eks. BF 3). Enzymkatalysert syntese (ved bruk av hydrolaser, proteaser og lipaser som katalysatorer) er også et godt alternativ (figur 8).
Den enzymkatalyserte syntesen av dilaurylated arginine-glyseridekonjugater ved bruk av papain er rapportert. Syntese av diacylglycerolesterkonjugater fra acetylarginin og evaluering av deres fysisk -kjemiske egenskaper er også rapportert.
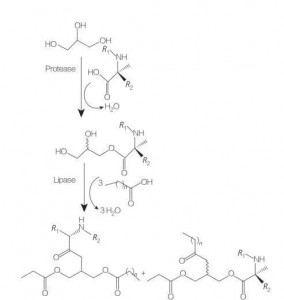
Fig.8 Syntese av mono og diacylglycerol aminosyrekonjugater
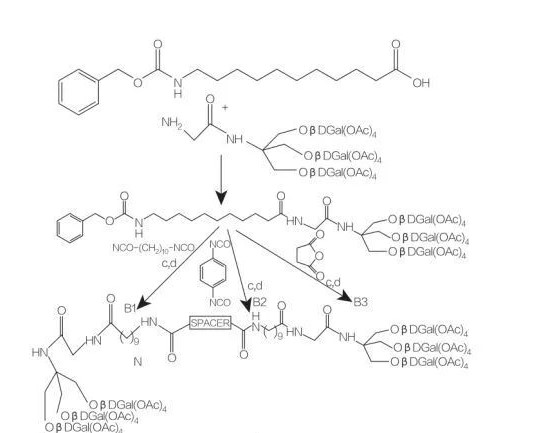
Spacer: NH- (Ch2)10-Nh: Compoundb1
Spacer: NH-C6H4-Nh: Compoundb2
Spacer: Ch2-CH2: COMPOUNDB3
Fig.9 Syntese av symmetriske amfifiler avledet fra Tris (hydroksymetyl) aminmetan
5.2.4 Syntese av bolbaserte aminosyre/peptidovergrepetanser
Aminosyrebaserte amfifiler av Bola-type inneholder 2 aminosyrer som er knyttet til den samme hydrofobe kjeden. Franceschi et al. beskrev syntesen av amfifiler av bola-type med 2 aminosyrer (D- eller L-alanin eller L-histidin) og 1 alkylkjede med forskjellige lengder og undersøkte deres overflateaktivitet. De diskuterer syntese og aggregering av nye amfifiler av Bola-type med en aminosyrefraksjon (ved bruk av enten en uvanlig ß-aminosyre eller en alkohol) og en C12 -C20 spacer-gruppe. De uvanlige ß-aminosyrene som brukes kan være en sukkeraminoacid, en azidothymin (AZT) -ledet aminosyre, en norborne aminosyre og en aminoalkohol avledet fra AZT (figur 9). Syntesen av symmetrisk bolatype amfifiler avledet fra Tris (hydroksymetyl) aminometan (Tris) (figur 9).
06 Fysisk -kjemiske egenskaper
Det er velkjent at aminosyrebaserte overflateaktive midler (AAS) er forskjellige og allsidige i naturen og har god anvendbarhet i mange bruksområder som god solubilisering, gode emulgeringsegenskaper, høy effektivitet, høy overflateaktivitetsytelse og god motstand mot hardt vann (kalsiumion -toleranse).
Basert på de overflateaktive egenskapene til aminosyrer (f.eks overflatespenning, CMC, faseatferd og KRAFFT -temperatur), ble følgende konklusjoner nådd etter omfattende studier - overflateaktiviteten til AAS er overlegen den for dens konvensjonelle overflateaktive motstykke.
6.1 Kritisk micellekonsentrasjon (CMC)
Kritisk micellekonsentrasjon er en av de viktige parametrene for overflateaktive midler og styrer mange overflateaktive egenskaper som solubilisering, cellelysering og dens interaksjon med biofilmer, etc. Generelt, øker kjedelengden på hydrokarbonhalen (økende hydrofobisitet) til en nedgang i CMC -verdien av den surfaktant -løsningen, og øker dens overflateaktivitet. Surfaktanter basert på aminosyrer har vanligvis lavere CMC -verdier sammenlignet med konvensjonelle overflateaktive stoffer.
Gjennom forskjellige kombinasjoner av hodegrupper og hydrofobe haler (monokationisk amid, bi-kationisk amid, bi-kationisk amidbasert ester), Infante et al. Syntetisert tre argininbaserte AA-er og studerte deres CMC og γCMC (overflatespenning ved CMC), og viste at CMC- og γCMC-verdiene falt med økende hydrofob halelengde. I en annen studie fant Singare og Mhatre at CMC for N-a-acylarginin-overflateaktive midler falt med å øke antallet hydrofobe karbonatomer (tabell 1).
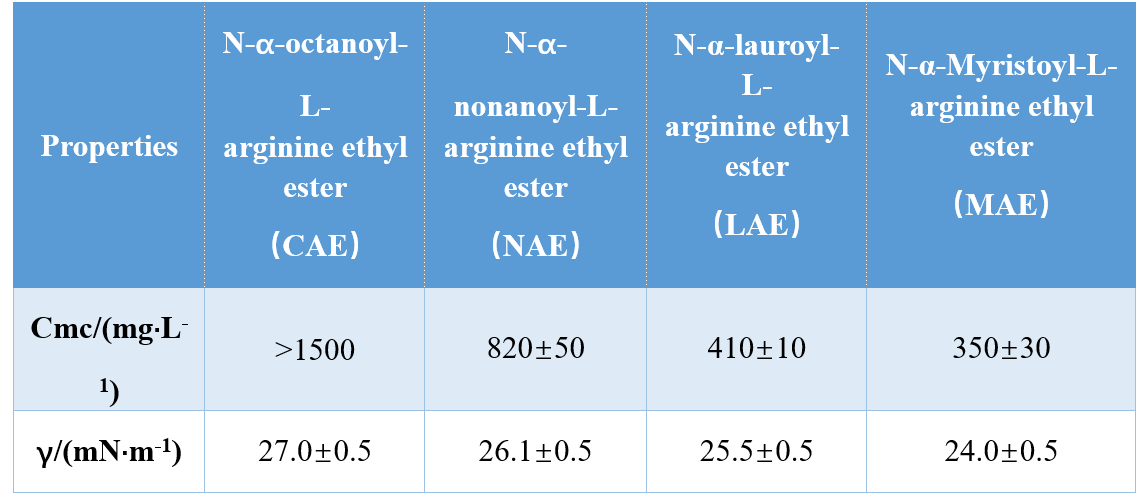
Yoshimura et al. Undersøkte CMC for cystein-avledede aminosyrebaserte Gemini-overflateaktive midler og viste at CMC reduserte når karbonkjedelengden i den hydrofobe kjeden ble økt fra 10 til 12. ytterligere å øke karbonkjedelengden til 14 resulterte i en økning i CMC, noe som bekreftet at langvarige gemini-surfaktanter hadde en en lavere tendens til å få en lavere.
Faustino et al. rapporterte dannelsen av blandede miceller i vandige oppløsninger av anioniske Gemini -overflateaktive midler basert på cystin. Gemini -overflateaktive midler ble også sammenlignet med de tilsvarende konvensjonelle monomere overflateaktive midler (C 8 Cys). CMC-verdiene for lipid-surfaktantblandinger ble rapportert å være lavere enn for rene overflateaktive midler. Gemini overflateaktive midler og 1,2-diieptanoyl-SN-glyceryl-3-fosfokolin, en vannoppløselig, micelldannende fosfolipid, hadde CMC i det millimolare nivået.
Shrestha og Aramaki undersøkte dannelsen av viskoelastiske ormlignende miceller i vandige oppløsninger av blandede aminosyrebaserte anioniske-nonioniske overflateaktive midler i fravær av blandingssalter. I denne studien ble N-dodecylglutamat funnet å ha en høyere Krafft-temperatur; Når den nøytraliserte med den basiske aminosyren L-lysin, genererte den imidlertid miceller, og løsningen begynte å oppføre seg som en Newtonsk væske ved 25 ° C.
6.2 God vannløselighet
Den gode vannløseligheten til AAS skyldes tilstedeværelsen av ytterligere co-NH-obligasjoner. Dette gjør AAS mer biologisk nedbrytbar og miljøvennlig enn de tilsvarende konvensjonelle overflateaktive midler. Vannløseligheten av N-Acyl-L-glutaminsyre er enda bedre på grunn av sine 2 karboksylgrupper. Vannløseligheten til CN (Ca) 2 er også god fordi det er 2 ioniske arginingrupper i 1 molekyl, noe som resulterer i mer effektiv adsorpsjon og diffusjon ved cellegrensesnittet og til og med effektiv bakteriell hemming ved lavere konsentrasjoner.
6.3 Krafft -temperatur og Krafft -punkt
Krafft -temperatur kan forstås som den spesifikke løselighetsatferden til overflateaktive midler hvis løselighet øker kraftig over en bestemt temperatur. Ioniske overflateaktive midler har en tendens til å generere faste hydrater, noe som kan utfelle ut av vannet. Ved en bestemt temperatur (den såkalte Krafft-temperaturen) observeres vanligvis en dramatisk og diskontinuerlig økning i løseligheten av overflateaktive midler. Krafft -punktet for et ionisk overflateaktivt middel er Krafft -temperaturen ved CMC.
Denne løselighetskarakteristikken sees vanligvis for ioniske overflateaktive midler og kan forklares som følger: Løseligheten av det overflateaktive fritt monomer er begrenset under Krafft -temperaturen til Krafft -punktet er nådd, der løseligheten gradvis øker på grunn av micelleformasjon. For å sikre fullstendig løselighet er det nødvendig å utarbeide overflateaktive formuleringer ved temperaturer over Krafft -punktet.
The Krafft temperature of AAS has been studied and compared with that of conventional synthetic surfactants.Shrestha and Aramaki studied the Krafft temperature of arginine-based AAS and found that the critical micelle concentration exhibited aggregation behavior in the form of pre-micelles above 2-5×10-6 mol-L -1 followed by normal micelle formation ( Ohta et al. synthesized six different types of N-HEXADECANOYL AAS og diskuterte forholdet mellom deres Krafft-temperatur og aminosyrerester.
I eksperimentene ble det funnet at Krafft-temperaturen til N-heksadecanoyl AAS økte med synkende størrelse på aminosyrerester (fenylalanin var et unntak), mens varmen av løselighet (varmeopptak) økte med avtagende størrelse på aminosyrerester (med unntak av glid og fenylalanin). Det ble konkludert med at i både alanin- og fenylalaninsystemer er DL-interaksjonen sterkere enn LL-interaksjonen i den faste formen til N-heksadecanoyl AAS-saltet.
Brito et al. Bestemte Krafft-temperaturen på tre serier av nye aminosyrebaserte overflateaktive midler ved bruk av differensiell skanningsmikrokalorimetri og fant at å endre trifluoracetation til jodidion resulterte i en betydelig økning i Krafft-temperatur (ca. 6 ° C), fra 47 ° C til 53 ° C. Tilstedeværelsen av cis-double bindinger og umettetheten som er til stede i de langkjedede ser-derivatene førte til en betydelig reduksjon i Krafft-temperaturen. N-dodecylglutamat ble rapportert å ha en høyere Krafft-temperatur. Imidlertid resulterte nøytralisering med den grunnleggende aminosyren L-lysin i dannelse av miceller i løsning som oppførte seg som Newtonian væsker ved 25 ° C.
6.4 Overflatespenning
Overflatespenningen til overflateaktive midler er relatert til kjedelengden på den hydrofobe delen. Zhang et al. bestemte overflatespenningen til natriumkokoylglykinat ved hjelp av Wilhelmy Plate -metoden (25 ± 0,2) ° C og bestemte overflatespenningsverdien ved CMC som 33 mN -M -1, CMC som 0,21 mmol -L -1. Yoshimura et al. bestemte overflatespenningen til aminosyrebasert overflatespenning på 2C N Cys type av 2C N Cys-baserte overflateaktive midler. Det ble funnet at overflatespenningen ved CMC falt med økende kjedelengde (til n = 8), mens trenden ble reversert for overflateaktive midler med n = 12 eller lengre kjedelengder.
Effekten av CAC1 2 på overflatespenningen til dikarboksylert aminosyrebaserte overflateaktive midler er også studert. I disse studiene ble CAC1 2 tilsatt vandige oppløsninger av tre dikarboksylerte aminosyretype overflateaktive midler (C12 Malna 2, C12 aspna 2 og C12 glun 2). Platåverdiene etter CMC ble sammenlignet, og det ble funnet at overflatespenningen avtok ved veldig lave CAC12 -konsentrasjoner. Dette skyldes effekten av kalsiumioner på arrangementet av overflateaktivt middel ved gass-vann-grensesnittet. Overflatespenningene til saltene av N-dodecylaminomalonat og N-dodecylaspartat, derimot, var også nesten konstante opp til 10 mmol-L -1 CAC12-konsentrasjon. Over 10 mmol -l -1 øker overflatespenningen kraftig på grunn av dannelsen av en nedbør av kalsiumsaltet til overflateaktivt middel. For desodiumsaltet av N-dodecylglutamat resulterte moderat tilsetning av CAC1 2 i en betydelig reduksjon i overflatespenning, mens fortsatt økning i CAC12-konsentrasjonen ikke lenger forårsaket signifikante endringer.
For å bestemme adsorpsjonskinetikken til Gemini-Type AAS ved gass-vann-grensesnittet, ble den dynamiske overflatespenningen bestemt ved bruk av den maksimale bobletrykksmetoden. Resultatene viste at for den lengste testtiden endret 2C 12 Cys dynamiske overflatespenningen ikke. Nedgangen av den dynamiske overflatespenningen avhenger bare av konsentrasjonen, lengden på de hydrofobe halene og antall hydrofobe haler. Økende konsentrasjon av overflateaktivt middel, synkende kjedelengde så vel som antall kjeder resulterte i et raskere forfall. Resultatene oppnådd for høyere konsentrasjoner av C N Cys (n = 8 til 12) ble funnet å være veldig nær y CMC målt ved Wilhelmy -metoden.
I en annen studie ble de dynamiske overflatespenningene til natriumdilauryl cystin (SDLC) og natriumdiedcamino cystin bestemt ved Wilhelmy -platemetoden, og i tillegg ble likevektsoverflatespenningene til deres vandige oppløsninger bestemt ved fallvolummetoden. Reaksjonen av disulfidbindinger ble også undersøkt ved andre metoder. Tilsetningen av merkaptoetanol til 0,1 mmol -L -1SDLC -løsning førte til en rask økning i overflatespenning fra 34 mN -M -1 til 53 mN -m -1. Siden NaClo kan oksidere disulfidbindinger av SDLC til sulfonsyregrupper, ble det ikke observert noen aggregater når NaClo (5 mmol -L -1) ble tilsatt til 0,1 mmol -L -1 SDLC -løsning. Overføringselektronmikroskopi og dynamiske lysspredningsresultater viste at ingen aggregater ble dannet i løsningen. Overflatespenningen til SDLC ble funnet å øke fra 34 mN -m -1 til 60 mN -m -1 over en periode på 20 minutter.
6.5 Binære overflateinteraksjoner
I biovitenskapene har en rekke grupper studert vibrasjonsegenskapene til blandinger av kationiske AA-er (diacylglycerol argininbaserte overflateaktive midler) og fosfolipider ved gass-vann-grensesnittet, til slutt konkluderer med at denne ikke-ideelle egenskapen forårsaker utbredelsen av elektrostatiske interaksjoner.
6.6 Aggregeringsegenskaper
Dynamisk lysspredning brukes ofte for å bestemme aggregeringsegenskapene til aminosyrebaserte monomerer og Gemini-overflateaktive midler i konsentrasjoner over CMC, noe som gir en tilsynelatende hydrodynamisk diameter DH (= 2R H). Aggregatene dannet av C n Cys og 2cn Cys er relativt store og har en bred skalafordeling sammenlignet med andre overflateaktive midler. Alle overflateaktive midler unntatt 2C 12 Cys danner vanligvis aggregater på omtrent 10 nm. Micelle størrelser av Gemini -overflateaktive midler er betydelig større enn de monomere kollegene. En økning i hydrokarbonkjedelengde fører også til en økning i micellestørrelse. Ohta et al. beskrev aggregeringsegenskapene til tre forskjellige stereoisomerer av N-dodecyl-fenyl-alanyl-fenyl-alanin tetrametylammonium i vandig løsning og viste at diastereoisomerer har den samme kritiske aggregeringskonsentrasjonen i vandig løsning. Iwahashi et al. investigated by circular dichroism, NMR and vapor pressure osmometry the The formation of chiral aggregates of N-dodecanoyl-L-glutamic acid, N-dodecanoyl-L-valine and their methyl esters in different solvents (such as tetrahydrofuran, acetonitrile, 1,4-dioxane and 1,2-dichloroethane) with rotational properties was undersøkt ved sirkulær dikroisme, NMR og damptrykk -osmometri.
6.7 Grensesnittadsorpsjon
Grensesnittadsorpsjonen av aminosyrebaserte overflateaktive midler og dens sammenligning med dens konvensjonelle motstykke er også en av forskningsretninger. For eksempel ble grensesnittadsorpsjonsegenskapene til dodecylestere av aromatiske aminosyrer oppnådd fra Let og LEP undersøkt. Resultatene viste at Let og LEP viste lavere grensesnittområder ved gass-væske-grensesnittet og ved henholdsvis vann/heksan-grensesnittet.
Bordes et al. undersøkte løsningsatferden og adsorpsjonen ved gass-vann-grensesnittet til tre dikarboksylerte aminosyreoverflater, desodiumsaltene av dodecylglutamat, dodecyl aspartat og aminomalonat (med henholdsvis 3, 2 og 1 karbonatomer mellom de to karboksylgruppene). I følge denne rapporten var CMC for de dikarboksylerte overflateaktive midlene 4-5 ganger høyere enn for det monokarboksylerte dodecylglycinsaltet. Dette tilskrives dannelsen av hydrogenbindinger mellom de dikarboksylerte overflateaktive midler og nærliggende molekyler gjennom amidgruppene der.
6.8 Faseatferd
Isotropiske diskontinuerlige kubiske faser blir observert for overflateaktive midler ved veldig høye konsentrasjoner. Surfaktantmolekyler med veldig store hodegrupper har en tendens til å danne aggregater av mindre positiv krumning. Marques et al. studerte faseoppførselen til 12lyS12/12Ser og 8lyS8/16Ser -systemene (se figur 10), og resultatene viste at 12lyS12/12Ser -system Faseområde). Det skal bemerkes at for vesikkelregionen i 12lyS12/12Ser -systemet, er vesikler alltid sameksisterende med miceller, mens vesikkelregionen i 8lyS8/16Ser -systemet bare har vesikler.
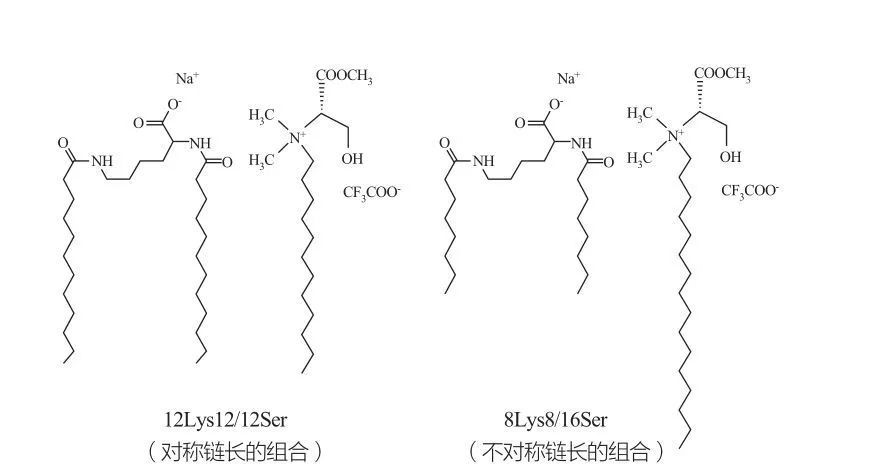
Katanioniske blandinger av det lysin- og serinbaserte overflateaktive midler: Symmetrisk 12lyS12/12Ser Pair (til venstre) og asymmetrisk 8lyS8/16Ser Pair (til høyre)
6.9 emulgeringsevne
Kouchi et al. undersøkte emulgeringsevnen, grensesnittspenningen, spredningen og viskositeten til N- [3-dodecyl-2-hydroxypropyl] -L-arginin, L-glutamat og andre AA-er. Sammenlignet med syntetiske overflateaktive midler (deres konvensjonelle ikke -ioniske og amfoteriske kolleger), viste resultatene at AAS har sterkere emulgeringsevne enn konvensjonelle overflateaktive midler.
Baczko et al. Syntetisert nye anioniske aminosyreoverflateaktive midler og undersøkte deres egnethet som chirale orienterte NMR -spektroskopi -løsningsmidler. En serie sulfonatbaserte amfifile L-Phe- eller L-Ala-derivater med forskjellige hydrofobe haler (pentyl ~ tetradecyl) ble syntetisert ved å reagere aminosyrer med O-sulfobenzoisk anhydrid. Wu et al. syntetiserte natriumsalter av N-fatty acyl AAs ogundersøkte deres emulgeringsevne i olje-i-vann-emulsjoner, og resultatene viste at disse overflateaktive midlene presterte bedre med etylacetat som oljefasen enn med N-heksan som oljefase.
6.10 Fremskritt i syntese og produksjon
Hardt vannmotstand kan forstås som overflateaktive midler til å motstå tilstedeværelsen av ioner som kalsium og magnesium i hardt vann, dvs. evnen til å unngå nedbør i kalsiumsåper. Surfaktanter med høy hard vannmotstand er veldig nyttige for vaskemiddelformuleringer og personlig pleieprodukter. Hardt vannmotstand kan evalueres ved å beregne endringen i løselighet og overflateaktivitet av overflateaktivt middel i nærvær av kalsiumioner.
En annen måte å evaluere hardt vannmotstand er å beregne prosentandelen eller gram overflateaktivt middel som kreves for kalsiumsåpen som er dannet fra 100 g natriumjeat som skal spres i vann. I områder med høyt hardt vann, kan høye konsentrasjoner av kalsium- og magnesiumioner og mineralinnhold gjøre noen praktiske anvendelser vanskelig. Ofte brukes natriumionet som tellerion av et syntetisk anionisk overflateaktivt middel. Siden det divalente kalsiumionet er bundet til begge overflateaktive molekyler, får det overflateaktivt middel til å utfelle lettere fra løsningsmessig vasking mindre sannsynlig.
Studien av den harde vannmotstanden til AAS viste at syre- og hardtvannsmotstanden var sterkt påvirket av en ekstra karboksylgruppe, og syre- og hardtvannsmotstanden økte ytterligere med økningen av lengden på avstandsgruppen mellom de to karboksylgruppene. Rekkefølgen av syre og hardt vannmotstand var C 12 glycinat <C 12 aspartat <C 12 glutamat. Sammenligning av den dikarboksylerte amidbindingen og det henholdsvis det dikarboksylerte aminoet overflateaktivt middel, ble det funnet at pH -området til sistnevnte var bredere og dens overflateaktivitet økte med tilsetning av en passende mengde syre. De dikarboksylerte N-alkylaminosyrene viste chelaterende effekt i nærvær av kalsiumioner, og C 12 aspartat dannet hvit gel. C 12 glutamat viste høy overflateaktivitet ved høy Ca 2+ konsentrasjon og forventes å bli brukt i avsalting av sjøvann.
6.11 Spredbarhet
Spredbarhet refererer til evnen til et overflateaktivt middel til å forhindre koalescens og sedimentering av overflateaktivt middel i løsning.Spredbarhet er en viktig egenskap av overflateaktive midler som gjør dem egnet for bruk i vaskemidler, kosmetikk og legemidler.Et dispergeringsmiddel må inneholde en ester, eter, amid eller aminobinding mellom den hydrofobe gruppen og den terminale hydrofile gruppen (eller blant de rette kjede hydrofobe gruppene).
Generelt er anioniske overflateaktive midler som alkanolamidosulfater og amfoteriske overflateaktive midler som amidosulfobetain spesielt effektive som spredningsmidler for kalsiumsåper.
Mange forskningsinnsatser har bestemt spredningen av AAS, der N-LaUoyl-lysin ble funnet å være dårlig kompatibel med vann og vanskelig å bruke til kosmetiske formuleringer.I denne serien har N-acyl-substituerte grunnleggende aminosyrer suveren spredbarhet og brukes i den kosmetiske industrien for å forbedre formuleringene.
07 Toksisitet
Konvensjonelle overflateaktive midler, spesielt kationiske overflateaktive midler, er svært giftige for vannlevende organismer. Deres akutte toksisitet skyldes fenomenet adsorpsjon-ion-interaksjon av overflateaktive midler ved cellevannsgrensesnittet. Å redusere CMC av overflateaktive midler fører vanligvis til sterkere grensesnittadsorpsjon av overflateaktive midler, noe som vanligvis resulterer i deres forhøyede akutte toksisitet. En økning i lengden på den hydrofobe kjeden av overflateaktive midler fører også til en økning i overflateaktivt middel akutt toksisitet.De fleste AA-er er lave eller ikke-giftige for mennesker og miljø (spesielt for marine organismer) og er egnet for bruk som matingredienser, legemidler og kosmetikk.Mange forskere har vist at aminosyre-overflateaktive midler er milde og ikke-irriterende for huden. Argininbaserte overflateaktive midler er kjent for å være mindre giftige enn deres konvensjonelle kolleger.
Brito et al. studerte de fysisk-kjemiske og toksikologiske egenskapene til aminosyrebaserte amfifiler og deres [derivater fra tyrosin (Tyr), hydroksyprolin (HYP), serin (ser) og lysin (Lys)] spontan formasjon av cationic vesicles og ga data på deres akutt til å være vant til DAPH til DAPH til DAPH til DAPH til DAPH (serin (serin (serin (serin (serin (serin (serin (serin (serin (serin (serin (serin (serin (serin (serin (serin (serin (serin). De syntetiserte kationiske vesikler av dodecyltriethylammonium bromid (DTAB)/lys-derivat og/eller ser-/lys-derivative blandinger og testet deres økotoksisitet og hemolytiske potensial, og viste at alle AAS og deres ves-knevende blanding var mindre toxic enn den konvensjonen som er vesigvakt, og deres vesvakt-konvensjoner og deres veske-konvensjoner var mindre.
Rosa et al. undersøkte bindingen (assosiasjonen) av DNA til stabile aminosyrebaserte kationiske vesikler. I motsetning til konvensjonelle kationiske overflateaktive midler, som ofte ser ut til å være giftig, ser interaksjonen mellom kationiske aminosyreoverflateaktive midler ut til å være giftig. Den kationiske AAS er basert på arginin, som spontant danner stabile vesikler i kombinasjon med visse anioniske overflateaktive stoffer. Aminosyrebaserte korrosjonshemmere er også rapportert å være ikke-giftige. Disse overflateaktive midlene syntetiseres lett med høy renhet (opptil 99%), lave kostnader, lett biologisk nedbrytbar og fullstendig løselig i vandige medier. Flere studier har vist at svovelholdige aminosyre-overflateaktive midler er overlegne i korrosjonshemming.
I en fersk studie har Perinelli et al. rapporterte en tilfredsstillende toksikologisk profil av rhamnolipider sammenlignet med konvensjonelle overflateaktive stoffer. Rhamnolipider er kjent for å fungere som permeabilitetsforsterkere. De rapporterte også om effekten av rhamnolipider på epitelpermeabiliteten til makromolekylære medisiner.
08 Antimikrobiell aktivitet
Den antimikrobielle aktiviteten til overflateaktive midler kan evalueres ved den minste hemmende konsentrasjonen. Den antimikrobielle aktiviteten til argininbaserte overflateaktive stoffer er blitt studert i detalj. Gram-negative bakterier ble funnet å være mer resistente mot argininbaserte overflateaktive midler enn gram-positive bakterier. Den antimikrobielle aktiviteten til overflateaktive midler økes vanligvis ved tilstedeværelsen av hydroksyl, syklopropan eller umettede bindinger i acylkjedene. Castillo et al. viste at lengden på acylkjedene og den positive ladningen bestemmer HLB-verdien (hydrofil-lipofil balanse) av molekylet, og disse har en effekt på deres evne til å forstyrre membraner. Nα-acylarginin metylester er en annen viktig klasse av kationiske overflateaktive midler med bredspektret antimikrobiell aktivitet, og den er lett biologisk nedbrytbar og har lav eller ingen toksisitet. Studier på interaksjonen mellom Nα-acylarginin metylesterbaserte overflateaktive midler med 1,2-dipalmitoyl-SN-propyltrioksyl-3-fosforylkolin og 1,2-DiteTradecanoyl-SN-Propyltrioxyl-3-fosforlcholin, modellmembraner og stuer i closfor-closfore, modellen i closfor-classylcholine, modellen, modellen, modellen, modellen, og 1,2-ditecanoyl-SN-propyltria-3-fosfor-av-ditecanoyl-SN-propyltriaxyl-3-fosforlinjene, som er en classy-3-fosfor. Surfaktanter har god antimikrobiell resultatene viste at overflateaktive midler har god antibakteriell aktivitet.
09 Revologiske egenskaper
De reologiske egenskapene til overflateaktive midler spiller en veldig viktig rolle i å bestemme og forutsi deres applikasjoner i forskjellige bransjer, inkludert mat, legemidler, oljeutvinning, personlig pleie og hjemmepleieprodukter. Mange studier har blitt utført for å diskutere forholdet mellom viskoelastisitet av aminosyre -overflateaktive midler og CMC.
10 applikasjoner i kosmetikkindustrien
AAS brukes i formuleringen av mange personlige pleieprodukter.Kalium N-cocoylglykinat er funnet å være skånsom mot huden og brukes i ansiktsrensing for å fjerne slam og sminke. N-Acyl-L-glutaminsyre har to karboksylgrupper, noe som gjør det mer vannløselig. Blant disse AA -ene er AAS basert på C 12 -fettsyrer mye brukt i ansiktsrensing for å fjerne slam og sminke. AAS med en C 18-kjede brukes som emulgatorer i hudpleieprodukter, og N-Lauryl alaninsalter er kjent for å skape kremete skum som ikke er irriterende for huden og kan derfor brukes til å formulere babypleieprodukter. N-Lauryl-baserte AA-er som brukes i tannkrem har god vaskekrav som såpe og sterk enzymhemmende effekt.
I løpet av de siste tiårene har valg av overflateaktive midler for kosmetikk, personlig pleieprodukter og legemidler fokusert på lav toksisitet, mildhet, mildhet til berøring og sikkerhet. Forbrukere av disse produktene er akutt klar over potensiell irritasjon, toksisitet og miljømessige faktorer.
I dag brukes AAS til å formulere mange sjampoer, hårfargestoffer og badesåper på grunn av deres mange fordeler i forhold til deres tradisjonelle kolleger innen kosmetikk og personlig pleieprodukter.Proteinbaserte overflateaktive midler har ønskelige egenskaper som er nødvendige for personlig pleieprodukter. Noen AA-er har filmdannende evner, mens andre har gode skummende evner.
Aminosyrer er viktige naturlig forekommende fuktighetsgivende faktorer i stratum corneum. Når epidermale celler dør, blir de en del av stratum corneum og de intracellulære proteinene blir gradvis degradert til aminosyrer. Disse aminosyrene blir deretter transportert videre inn i stratum corneum, hvor de absorberer fett eller fettlignende stoffer inn i epidermal stratum corneum, og dermed forbedrer elastisiteten i hudens overflate. Omtrent 50% av den naturlige fuktighetsgivende faktoren i huden er sammensatt av aminosyrer og pyrrolidon.
Kollagen, en vanlig kosmetisk ingrediens, inneholder også aminosyrer som holder huden myk.Hudproblemer som ruhet og sløvhet skyldes i stor grad mangel på aminosyrer. En studie viste at blanding av en aminosyre med en salve lettet hudforbrenninger, og de berørte områdene kom tilbake til normal tilstand uten å bli keloid arr.
Aminosyrer har også vist seg å være veldig nyttige for å ta vare på skadede neglebånd.Tørt, formløst hår kan indikere en reduksjon i konsentrasjonen av aminosyrer i et sterkt skadet stratum corneum. Aminosyrer har evnen til å trenge gjennom kutikula i hårskaftet og absorbere fuktighet fra huden.Denne evnen til aminosyrebaserte overflateaktive midler gjør dem veldig nyttige i sjampo, hårfargestoffer, hårmykner, hårbalsam og tilstedeværelsen av aminosyrer gjør håret sterkt.
11 applikasjoner i hverdagskosmetikk
For øyeblikket er det en økende etterspørsel etter aminosyrebaserte vaskemiddelformuleringer over hele verden.AAS er kjent for å ha bedre rengjøringsevne, skummingsevne og mykgjørende egenskaper, noe som gjør dem egnet for husholdningsvaskemidler, sjampo, kroppsvask og andre bruksområder.En asparaginsyre-avledede amfoteriske AAS er rapportert å være et svært effektivt vaskemiddel med chelaterende egenskaper. Bruken av vaskemiddelingredienser bestående av N-alkyl-ß-aminoetoksysyrer ble funnet å redusere hudirritasjonen. En flytende vaskemiddelformulering bestående av N-cocoyl-ß-aminopropionat har blitt rapportert å være et effektivt vaskemiddel for oljeflekker på metalloverflater. Et aminokarboksylsyre-overflateaktivt middel, C 14 Chohch 2 NHCH 2 Coona, har også vist seg å ha bedre vask og brukes til å rengjøre tekstiler, tepper, hår, glass, etc. 2-hydroksy-3-aminopropionic acid-n, n-acetoedicic acent.
Fremstilling av vaskemiddelformuleringer basert på N- (N'-lang-kjede acyl-ß-alanyl) -p-alanin er rapportert av Keigo og Tatsuya i deres patent for bedre vaskeevne og stabilitet, lett skumbrudd og god mykgjøring av stoffer. KAO utviklet en vaskemiddelformulering basert på N-Acyl-1-N-hydroxy-ß-alanin og rapporterte lav hudirritasjon, høy vannmotstand og høy flekkfjerningskraft.
Det japanske selskapet Ajinomoto bruker lavtoksisk og lett nedbrytbar AAS basert på L-glutaminsyre, L-arginin og L-lysin som hovedingredienser i sjampoer, vaskemidler og kosmetikk (figur 13). Evnen til enzymtilsetningsstoffer i vaskemiddelformuleringer til å fjerne proteinforbindelse er også rapportert. N-acyl AAS avledet fra glutaminsyre, alanin, metylglycin, serin og asparaginsyre er rapportert for deres bruk som utmerkede flytende vaskemidler i vandige oppløsninger. Disse overflateaktive midlene øker ikke viskositeten i det hele tatt, selv ved svært lave temperaturer, og kan lett overføres fra lagringsbeholderen til skummingsanordningen for å oppnå homogene skum.
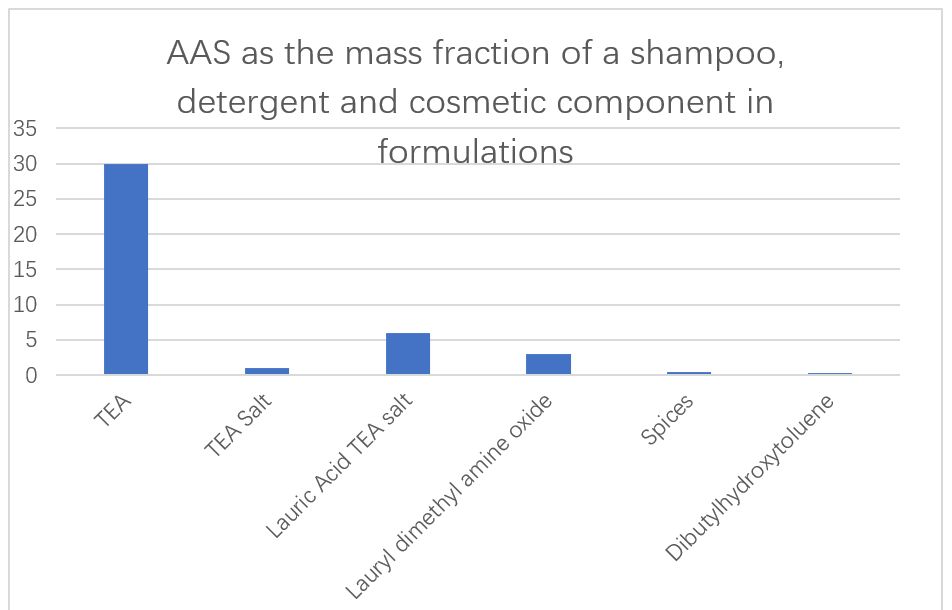
Post Time: Jun-09-2022

